服务热线
86-21-54488867 / 4008202557
GB/T 15072.6-2025 贵金属合金化学分析方法 第6部分:铱含量的测定
范围
本文件描述了硫酸亚铁电位滴定法测定贵金属合金中铱含量的测定方法。
本文件适用于贵金属合金中铱含量的测定。测定范围(质量分数):5.00%~30.00%。
术语和定义
本文件没有需要界定的术语和定义。
原理
试料置于聚四氟乙烯消化罐中,加盐酸与H2O2,于烘箱中加热溶解。钌元素用溴酸钠氧化钌与基体分离,钯元素用铜粉还原钯与基体分离。在盐酸和硫酸介质中,用硫酸亚铁标准滴定溶液滴定将Ir(Ⅳ)还原至Ir(Ⅲ),电位法指示终点以测定铱含量。
试剂和材料
除非另有说明,在分析中仅使用确认为分析纯的试剂和蒸馏水或去离子水或相当纯度的水。
KClO3固体(优级纯)。
铜粉:称取1.0g锌粉于100mL烧杯中,加1mL~2mL水润湿。加10mL硫酸铜溶液(197g/L),摇动2min~3min,加30mL盐酸。当剧烈反应停止后,倾滗上层溶液,加40mL盐酸浸泡1h。倾滗上层溶液,用水清洗4次,倒去上层溶液。所得的活性铜粉供还原1份溶液使用。用时现配。
盐酸(ρ=1.19g/mL)。
H2O2(ρ=1.10g/mL)。
硫酸溶液(1+1)。
硫酸溶液(4+96)。
氯化钠饱和溶液。
氯酸钠溶液(100g/L)。
溴化钠溶液(100g/L)。
硫酸亚铁标准滴定溶液[c(FeSO4•7H2O)约0.0011mol/L],按以下步骤配制和标定:
a) 配制:称取0.318g硫酸亚铁,溶入1000mL硫酸溶液中,混匀。
b) 标定:标定与试料的测定平行进行。移取10.00mL铱标准溶液3份,分别置于3个100mL高型烧杯中,各加入1滴氯酸钠溶液,5mL盐酸,混匀,静置约10min。加入0.5mL氯化钠饱和溶液、5mL硫酸溶液,加水至总体积约30mL。插入吹气管,于吹气装置上吹气10min,取下,用约10mL水冲洗吹气管和高型烧杯壁,再重复吹气10min。
将溶液转入120mL滴定杯中。
将滴定杯放在滴定转盘上,启动自动电位滴定仪,将已连接在自动电位滴定仪上的电极和滴定管插入样品溶液中,搅拌至少20s(设备参考参数见附录A)。用硫酸亚铁标准滴定溶液进行电位滴定至终点。从电位滴定曲线或dE/dV 曲线确定终点。记录终点所消耗的硫酸亚铁标准溶液体积V2。
平行标定3份,其标定所消耗硫酸亚铁标准滴定溶液体积的极差值应不超过0.05mL,取其平均值。
按公式(1)计算硫酸亚铁标准滴定溶液的实际浓度:![]()
式中:
c ——硫酸亚铁标准滴定溶液的实际浓度,单位为摩尔每毫升(mol/mL);
ρ0——铱标准溶液的质量浓度,单位为毫克每毫升(mg/mL);
V1——移取铱标准溶液的体积,单位为毫升(mL);
192.22——铱的摩尔质量,单位为克每摩尔(g/mol);
V2——标定时,滴定铱标准溶液所消耗硫酸亚铁标准滴定溶液的体积,单位为毫升(mL)。
铱标准溶液:称取0.10g铱粉(ωIr≥99.99%),精确至0.00001g,于50mL硬质玻璃封管,加入10mL盐酸,700mg KClO3置于气体反应支架内,气体反应支架置于硬质玻璃封管中,于300°C溶解至少6h。将管内试液移入200mL容量瓶中,用水冲洗4次~5次,加入100mL盐酸,用水稀释至刻度。混匀。此溶液1mL含0.5mg铱。
仪器设备
天平:感量0.01mg。
滴定装置:自动电位滴定仪。仪器工作参考参数见附录A。
聚四氟乙烯消化罐: 壁厚25mm±2mm,容积30mL,达到以上条件的消化罐均可使用。
烘箱(温度不大于300°C)。
恒温磁力搅拌器。
吹气装置,如图1所示。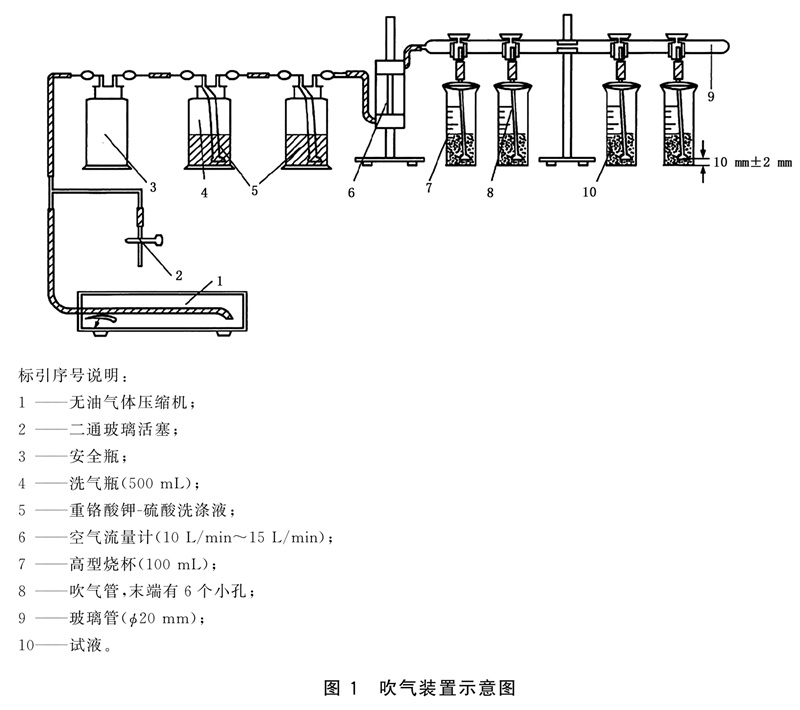
样品
样品加工成碎屑,碎屑的厚度不大于0.2mm,长度、宽度不大于2.0mm。用冰醋酸浸泡10min后,再用无水乙醇洗净、晾干,混匀。
试验步骤
试料
称取0.1g样品,精确至0.00001g。
平行试验
平行做两份试验,取其平均值。
空白试验
随同试料做空白试验。
测定
试样溶解
将试料置于聚四氟乙烯消化罐中,加20mL盐酸、5mL H2O2,密封聚四氟乙烯消化罐,于烘箱中150°C±5°C溶解36h。待冷却至室温,铱含量不大于10%的试液转入50mL容量瓶中,铱含量>10%的试液转入100mL容量瓶中,以水稀释至刻度,混匀。
试液的处理
不含钌和钯试液的处理
移取20mL试液于100mL高型烧杯中,加入5mL盐酸、5mL硫酸溶液、0.5mL氯化钠饱和溶液。
含钌试液的处理
移取20mL试液于100mL烧杯,加0.5mL氯化钠饱和溶液,蒸至湿盐状。加入约1mL水,再次蒸至湿盐状,反复2次。加入0.5mL溴酸钠溶液蒸至近干,重复3次。加入5mL盐酸将沉淀溶解,冲洗表面皿和杯壁,将溶液浓缩至体积约1mL,将溶液转入聚四氟乙烯消化罐中,加7mL盐酸、1.5mL H2O2,密闭聚四氟乙烯消化罐,置于烘箱中150°C±5°C溶解6h。取出,冷却至室温,将试液转入100mL高型烧杯中,加入5mL盐酸、5mL硫酸溶液。
含钯试液的处理
移取20mL试液于100mL烧杯中,置于电炉上,低温蒸发至2mL,取下。加40mL盐酸和铜粉,将烧杯放入恒温磁力搅拌器上的水浴皿中,在50°C~60°C 的水浴中加热搅拌30min,取下。用中性滤纸过滤,滤液滤入200mL烧杯中,用盐酸洗涤烧杯及沉淀4次~5次,弃去沉淀。滤液于电炉上低温蒸发至5mL,加入10mL盐酸、2mL氯酸钠溶液,盖上表面皿,再煮沸至5mL,取下。试液转入100mL 高型烧杯中,用盐酸洗涤烧杯壁和表面皿,每次2mL,再用水冲洗4次,每次约2.5mL。加1mL氯酸钠溶液,混匀。静置10min,加入20mL硫酸溶液。
含钌和钯试液的处理
移取20mL试液于100mL烧杯,加0.5mL氯化钠饱和溶液,蒸至湿盐状。加入约1mL水,再次蒸至湿盐状,反复2次。加入0.5mL溴酸钠溶液蒸至近干,重复3次。加入5mL盐酸将沉淀溶解,冲洗表面皿和杯壁,将溶液浓缩至体积约2mL,取下。加40mL盐酸和铜粉,将烧杯放入恒温磁力搅拌器上面的水浴皿中,在50°C~60°C的水浴中加热搅拌30min,取下。用中性滤纸过滤,滤液滤入200mL烧杯中,用盐酸洗涤烧杯及沉淀4次~5次,弃去沉淀。
滤液于电炉上低温蒸发至1mL,将溶液转入聚四氟乙烯消化罐中,加7mL盐酸、1.5mL H2O2,密闭聚四氟乙烯消化罐,置于烘箱中150°C±5°C溶解6h。取出,冷却至室温,将试液转入100mL高型烧杯中,加入5mL盐酸、5mL硫酸溶液。
吹气
于试液中,插入吹气管,在吹气装置上吹气。先吹气10min,用约10mL水冲洗高型烧杯壁和吹气管,再吹气10min,取下。用约5mL水冲洗吹气管和高型烧杯,重复3次,将试液转入120mL滴定杯中。
滴定
将滴定杯放在滴定转盘上,启动自动电位滴定仪,将已连接在自动电位滴定仪上的电极和滴定管插入样品溶液中,搅拌至少20s(设备参考参数见附录A),用硫酸亚铁标准滴定溶液进行电位滴定至终点。从电位滴定曲线或dE/dV曲线确定终点。记录终点所消耗的硫酸亚铁标准滴定溶液体积。
试验数据处理
铱含量以依的质量分数ωIr计,按公式(2)计算:![]()
式中:
c ——硫酸亚铁标准滴定溶液的实际浓度,单位为摩尔每毫升(mol/mL);
V5——滴定试液所消耗的硫酸亚铁标准滴定溶液的体积,单位为毫升(mL);
V0——滴定空白所消耗的硫酸亚铁标准滴定溶液的体积,单位为毫升(mL);
V3——试液总体积,单位为毫升(mL);
192.22——铱的摩尔质量,单位为克每摩尔(g/mol);
m0——试料的质量,单位为克(g);
V4——分取试液体积,单位为毫升(mL)。
试验结果的数值按 GB/T 8170 的规定进行修约,计算结果表示到小数点后两位。
京都电子KEM 自动电位滴定仪 AT-710S