服务热线
86-21-54488867 / 4008202557
T/ZZB 2168-2021 恩诺沙星
范围
本文件规定了恩诺沙星的基本要求、技术要求、试验方法、检验规则、标签、包装、运输和贮存、质量承诺等。
本文件适用于化学合成的恩诺沙星。
分子式:C19H22FN3O3
相对分子量:359.40(按2016年国际相对原子质量)
结构式: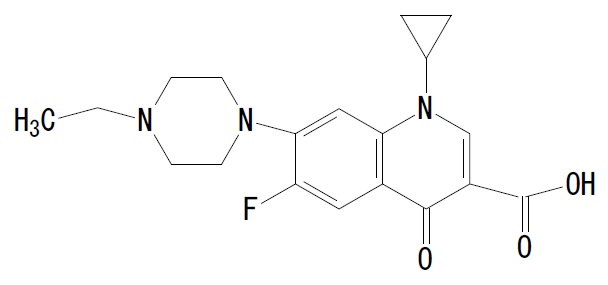
术语与定义
本文件没有需要界定的术语与定义。
基本要求
研发设计
应开展合成、除盐和除杂等关键工艺优化的研发设计工作,保证产品杂质B达到要求。
原材料
N-乙基Piperazine色谱纯度应不小于99.0%,杂质Piperazine应不大于0.2%。
氟氯苯乙酮色谱纯度应不小于99.0%,杂质三氯苯乙酮应不大于0.05%。
工艺及设备
应采用DCS自动控制系统、密闭固体投料器、转料器、自动上料机等设备。
应采用纳滤、树脂吸附工艺处理废水。
检验检测
应开展原材料主含量及杂质的检测。
应开展成品氟喹啉酸、有关物质、重金属、硫酸盐和氯化物检验项目的检测。
应采用红外光谱仪、气相色谱仪和高效液相色谱仪等设备。
技术要求
性状
外观
本品为微黄色或淡橙黄色结晶性粉末;无臭;遇光色渐变为橙红色。
溶解性
本品在Trichloromethane中易溶;在二甲基甲酰胺中略溶;在甲醇中微溶;在水中极微溶解;在*试液中微溶。
熔点
本品的熔点为(221~226)℃,熔融时同时分解。
鉴别
按规定的方法测试时,色谱图中供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
本品的红外光吸收图谱应与对照的图谱(见附录A)一致。
质量要求
应符合表1的要求。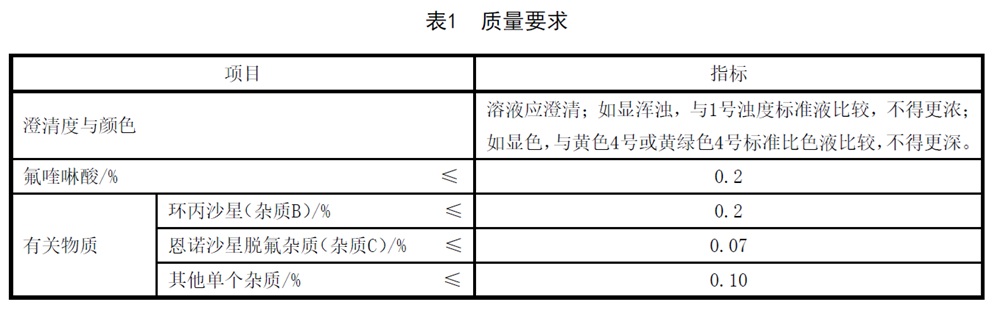
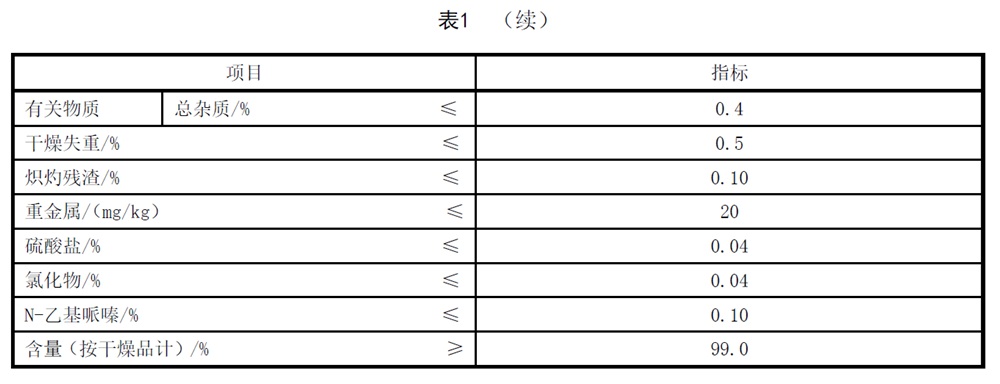
试验方法
含量
方法1
按《中华人民共和国兽药典》规定的方法执行。
方法2
取本品约0.25g,精密称定,加冰乙酸溶解后,用高氯酸滴定液(0.1mol/L)按《中国人民共和国兽药典》中附录0701电位滴定法与永停滴定和0702非水滴定通则规定执行。每1mL高氯酸滴定液(0.1mol/L)相当于35.94mg的C19H22FN3O3。
京都电子KEM 电位滴定法自动电位滴定仪 AT-710S